乾癬を緩和する生理活性脂質を生成する酵素の発見
本研究では、東京都医学総合研究所の平林哲也研究員らとの共同研究により、①マウス乾癬モデルの皮膚において抗炎症作用を持つ脂質メディエーターであるN-アシルエタノールアミン(NAE)の産生が増加すること、②リン脂質代謝酵素の一つである細胞質型ホスホリパーゼA2ε(cPLA2ε)が発現誘導されNAEの産生調節に関わること、③NAEがヒト皮膚角化細胞において炎症物質であるS100A9の発現を抑制し乾癬炎症を緩和させる作用があることを発見した。本結果は、これまで不明だった生体内でのNAEの産生経路とその乾癬病態における役割を初めて示したものである。皮膚におけるcPLA2εの発現誘導はマウス乾癬モデルだけでなくヒト乾癬患者でも認められることから、cPLA2εやNAEを標的とした創薬は乾癬の新たな治療に役立つ可能性が期待できる。
Luyiyun Liang*, Rina Takamiya*, Yoshimi Miki, Kanako Heike, Yoshitaka Taketomi, Nao Sugimoto, Midori Yamaguchi, Hiroshi Shitara, Yasumasa Nishito, Tetsuyuki Kobayashi, Tetsuya Hirabayashi, Makoto Murakami.
*Luyiyun Liang and Rina Takamiya contributed equally to this work.
Group IVE cytosolic phospholipase A2 limits psoriatic inflammation by mobilizing the anti-inflammatory lipid N-acylethanolamine.
FASEB J., 36, e22301 (2022).
AMEDプレス発表はこちら (2022/05/10)
東大プレス発表はこちら (2022/05/10)
日本経済新聞記事はこちら (2022/05/10)
1.研究の背景
皮膚は全身の体表を覆う臓器であり、外界から生体を保護するバリア機能(皮膚バリア)を担っている。脂質は皮膚バリアに必須の生体成分であり、脂質代謝の異常は皮膚バリアの破綻と皮膚疾患の形成につながることが報告されている。
乾癬は、皮膚の新陳代謝のサイクルが早くなることで皮膚が赤くなって盛り上がり、表面に白色の乾いた角質(角化細胞)が増生を来す慢性の炎症性角化症である。近年、Th17免疫応答を標的とした抗体医薬が乾癬の治療に効果を上げているが、高価な薬剤を永続的に投与し続けなければならず、安価な新薬の開発や根本的な要因の解明が求められている。
我々は長年にわたり脂質の代謝に関わる酵素群の研究を行ってきた。本研究では、マウスにおける乾癬モデルの網羅的な脂質プロファイリング解析で乾癬病態に相関して産生される脂質の探索を行い、乾癬の進行を抑える新しい脂質代謝経路を同定した。
2.研究内容
今回、マウスの皮膚に乾癬惹起剤であるイミキモドを塗布して経時的な網羅的脂質解析(リピドミクス解析)を行うことで、抗炎症作用を持つ脂質メディエーターであるNAEの多くの分子種の産生が病態の推移と相関して増加することを見つけた。これまで、試験管内においてNAEの生成に関わる酵素がいくつか報告されていたが、生体内での機能は不明であった。これらの酵素のうち、cPLA2εの発現のみが乾癬病態の推移と相関していた。また、cPLA2εの乾癬皮膚での発現は、ヒトとマウスの双方において表皮角化細胞の上層部に見られた(図1−①)。
cPLA2εは、ホスファチジルコリン(PC)のsn-1位の脂肪酸をホスファチジルエタノールアミン(PE)のアミノ基に転移してN-アシルPE(NAPE; NAEの前駆体)を生成するN-アシルトランスフェラーゼ反応を触媒する(図2)。そこで、上記の結果(図1−①)を受けて、我々はcPLA2εの遺伝子を人為的に欠損したノックアウトマウスを作製して乾癬モデルの表現型を解析した。その結果、ノックアウトマウスでは野生型マウスと比べて皮膚の肥厚が悪化するとともに、角化細胞の活性化マーカーであるS100a9やTh17免疫応答に関わるサイトカインであるIl17aの発現が亢進しており、乾癬病態の増悪が認められた。リピドミクス解析の結果、cPLA2εノックアウトマウスの皮膚では正常時から多くのNAE分子種の産生が顕著に低下しており、イミキモド塗布による乾癬惹起後のNAEの増加もほとんど認められなかった(図1−②)。このことから、乾癬病態におけるNAE産生の大部分は、cPLA2εにより制御されていることが分かった。次に、NAEに乾癬を抑える作用があるか検証したところ、マウス皮膚にNAEを塗布すると乾癬に伴う皮膚の肥厚や乾癬マーカー(S100a9、Il17a)の発現が低下し、また、ヒト培養角化細胞にNAEを添加すると乾癬関連サイトカインによるS100A9の発現誘導が抑えられた(図1−③)。
以上の結果から、乾癬病態で増加するNAEはcPLA2εによりその生成が制御されており、角化細胞の異常活性化を抑制することによって抗乾癬作用を示すことが分かった。
3.本研究の意義・今後の予定
本研究は、生体組織におけるNAE産生にリン脂質代謝酵素cPLA2εが関わること、並びに、本経路で産生されるNAEが乾癬の病態にブレーキをかける役割を担うことを初めて明らかにしたものである。NAEは乾癬病態における角化細胞の異常活性化を抑制する効果があることから、cPLA2εやNAEを標的とした創薬は乾癬の治療に役立つ可能性が期待できる。
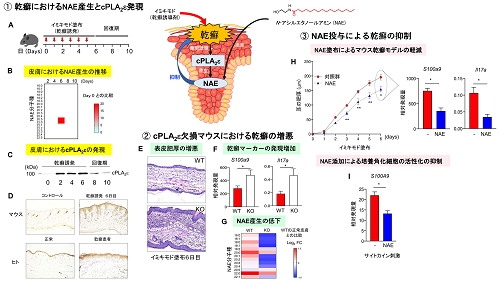
【図1】
cPLA2εは抗炎症性脂質メディエーターであるNAEの産生を介して乾癬を抑える。
①NAEの産生は、マウス皮膚にイミキモドを塗布して乾癬を惹起すると増加し、イミキモド塗布を止めて回復期に入ると低下する(A、B)。リン脂質代謝酵素であるcPLA2εの発現は、乾癬の進行に伴って皮膚に誘導され回復期に減少する(C)。マウスおよびヒトの乾癬皮膚において、cPLA2εは表皮角化細胞の上層部に発現している(D)。
②cPLA2εノックアウトマウス(KO)では、野生型マウス(WT)と比べてイミキモド塗布による耳介の肥厚が悪化し(E)、乾癬マーカーの発現が増加し(F)、NAEの産生が減少する(G)。
③イミキモド誘導乾癬モデルのマウス耳にNAEを塗布すると耳介の肥厚と乾癬マーカーの発現が低下し(H)、培養角化細胞にNAEを添加すると乾癬関連サイトカインの刺激による乾癬マーカーS100A9の発現誘導が抑えられる(I)。
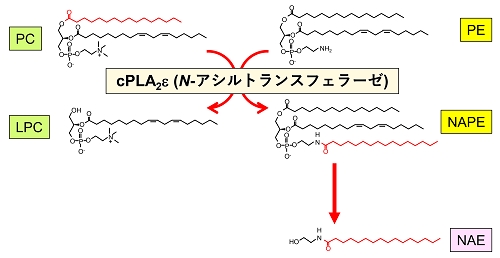
【図2】
cPLA2εは、ホスファチジルコリン(PC)のsn-1位の脂肪酸をホスファチジルエタノールアミン(PE)のアミノ基に転移してリゾホスファチジルコリン(LPC)とN-アシルPE(NAPE)を生成する(N-アシルトランスフェラーゼ反応)。NAPEがさらに別の酵素(皮膚では未同定)による加水分解を受けるとNAEが生成される。

 English
English ホーム
ホーム 研究紹介
研究紹介 研究業績
研究業績 日本語解説
日本語解説 メンバー
メンバー 研究室ドキュメント
研究室ドキュメント コラム
コラム